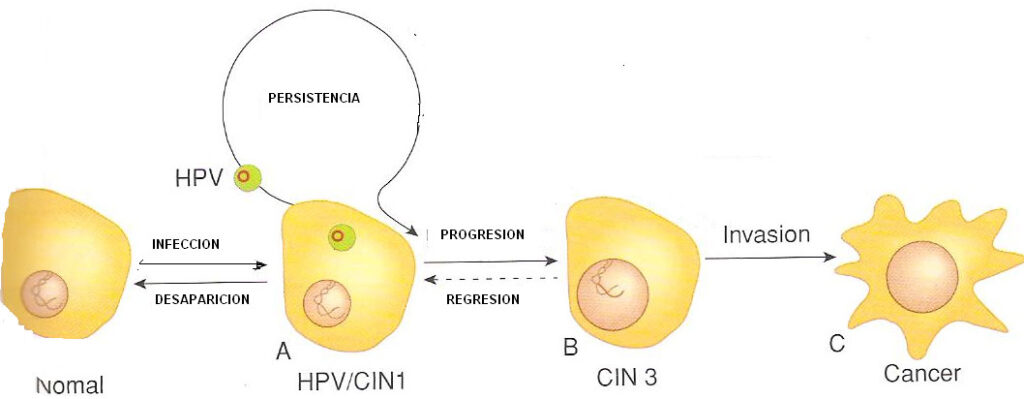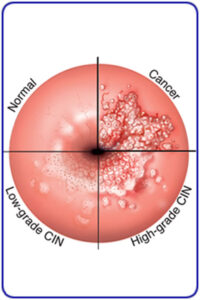

Es una enfermedad de transmisión sexual. La causa principal es la infección por virus del papiloma humano de alto riesgo. En el mundo se diagnostican anualmente 528.000 casos de cancer de cervix invasivo, de éstos 266.000 fallecen por esta causa. En España cada año mueren 1500 mujeres por esta enfermedad.
Todas estas muertes se pueden evitar si se efectúa periódicamente, (en mujeres sexualmente activas) una toma y lectura de citología cervicovaginal acompañada del genotipo HPV por PCR en cérvix uterino. La organización mundial de la salud WHO, la sociedad americana de oncología (ASCO) recomiendan que para la detección precoz del cancer de cérvix se realice un genotipado del Virus del Papiloma Humano antes que la citología. Si el genotipado dá positivo realizar citología.
Es importante seguir los consejos y las medidas apropiadas en el caso de que se presente alguna alteración, para evitar posibles efectos letales. El varón generalmente es portador asintomático. Así como en la mujer la toma para detectar el HPV por PCR tiene una sensibilidad y especificidad superior al 99 %, en el varón estos parámetros quedan reducidos aproximadamente al 50 % según los hábitos sexuales.
El preservativo NO protege de la transmisión del HPV.
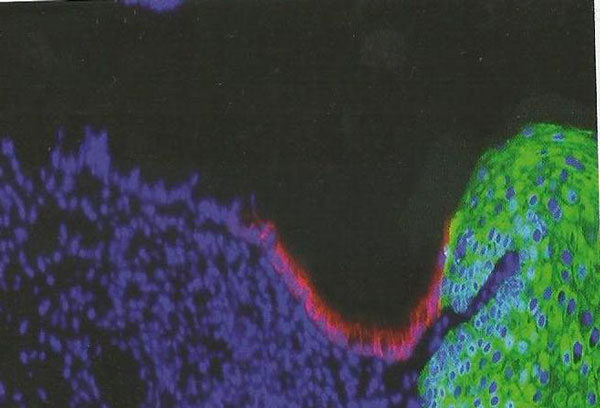
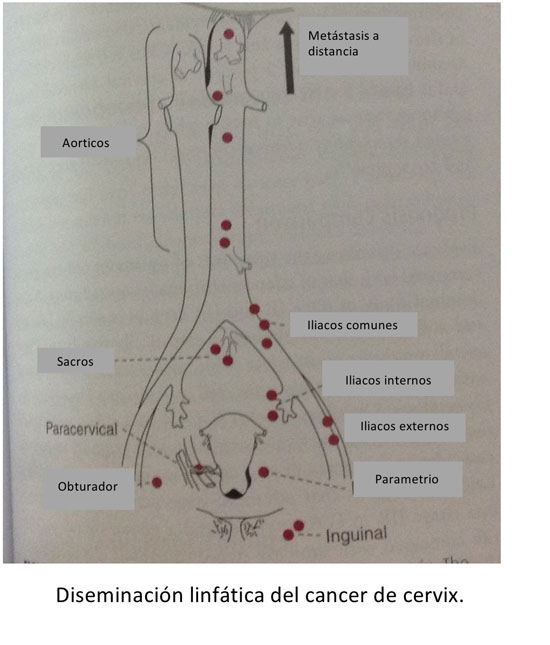
El cáncer de cérvix generalmente se inicia en la zona de transformación del cérvix (unión escamoso columnar) y se extiende hacia parametrios y ganglios linfáticos regionales.
El sistema Bethesdea establece 4 categorías de alteraciones citológicas cervicales:
- ASC-US: Celulas atípicas escamosas de significado indeterminado.
- LSIL: Lesión escamosa intraepitelial de bajo grado.
- HSIL: Lesión escamosa intraepitelial de alto grado.
- Células atípicas glandulares, una subcategoría de ASC que no descarta lesiones intraepiteliales escamosas de alto grado (ASC-H)
- Clasificación de las lesiones premalignas de cuello uterino:
| Displasia leve | CIN 1 | SIL de bajo grado (LSIL) |
| Displasia moderada | CIN 2 | Carcinoma in situ |
| Displasia severa | CIN 3 | SIL de alto grado (HSIL) |
CIN: Neoplasia cervical intraepitelial.
LSISL: Neoplasia cervical intraepitelial de bajo grado.
SIL: Lesión escamosa intraepitelial.
HSIL: Neoplasia cervical intraepitelial de alto grado
En el sistema Bethesda se sustituye el término neoplasia intraepitelial por el de lesión escamosa intraepitelial (SIL), con dos categorías: bajo grado (LSIL) y alto grado (HSIL). Esta división en dos grupos se justifica por la evidencia que las LSIL corresponden a infecciones víricas, en general autolimitadas y que sólo excepcionalmente progresan a carcinoma, mientras que las HSIL equivalen a verdaderos cambios premalignos que se corresponden con los siguientes términos utilizados en clasificaciones anteriores: Displasia moderada (CIN 2), displasia severa (CIN 3) y carcinoma in situ: La determinación del tipo de VPH en las lesiones intraepiteliales ha demostrado que en las LSIL se identifican tipos muy heterogéneos, de alto y bajo riesgo oncogénico, mientras que en la gran mayoría de HSIL se hallan tipos de alto riesgo.
Clasificación citológica de Bethesda, 2001: resultados e interpretaciones:
- Negativo para lesión intraepitelial o malignidad: Cuando no existe evidencia celular de neoplasia, aunque existan otros hallazgos no neoplásicos como microorganismos.
- Células epiteliales anormales.
¿Qué significa ASC-US?
- Son células escamosas de significado indeterminado (ASC-US) (atypical squamous cells of undertermined significance). Indican que son sugestivas pero no tienen los criterios de SIL. Aproximadamente entre un 5 y un 10% resultarán en un CINII o CINIII. El cáncer se presenta en un 2% de los casos.
- Que no pueden excluir lesión escamosa intraepitelial de alto grado (ASC-H) (atypical squamous cells high-grade). Describe cambios celulares que no son típicos del HSIL pero que no descartarse que sea una lesión de alto grado. En un 25% de estos pacientes se encontrarán HSIL.
- Lesión escamosa intraepitelial de bajo grado (LSIL) (low grade squamous intraepithelial lesión), Incluye infección por VHP/ displasia leve / CIN 1 (cervical intraepithelial neoplasia de grado 1)
- Lesión escamosa intraepitelial de alto grado (HSIL) (high grade squamous intraepithelial lesion) Incluye displasia moderada y severa / CIN 2 (cervical intrepithelial neoplasia de grado 2) y CIN 3 (cervical intraepithelial neoplasia de grado 3) / carcinoma escamoso in situ.
- Con características sospechosas de invasión.
- Si se sospecha invasión.
- Carcinoma escamoso.
Células Glandulares.
- Células glandulares atípicas (AGC) (atypical glandular cells): células endocervicales, células endometriales o células glandulares sin especificar origen.
- Células glandulares atípicas, posiblemente neoplásicas.
- Adenocarcinoma endocervical in situ (AIS).
- Adenocarcinoma endocervical, endometrial, extrauterino o sin especificar.
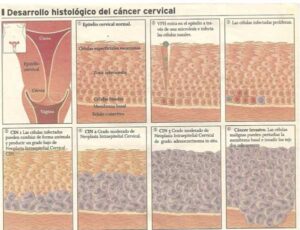
Introducción:
El virus del papiloma humano (VPH) representa una de las infecciones de transmisión sexual más comunes, aunque todavía poco conocida. La familia de los VPHs cuenta con más de 150 tipos virales que, en relación a su patogenia oncológica, se clasifican en tipos de alto y de bajo riesgo oncológico. Las infecciones por tipos de alto riesgo siguen predominantemente un curso silente, tienden a establecer infecciones persistentes y generan alteraciones citológicas características englobadas mayoritariamente en el grupo de las neoplasias cervicales de grado 1 (CIN 1), o lesiones escamosas intraepiteliales de bajo grado (LSIL). En una proporción menor, las infecciones por VPH de alto riesgo pueden progresar a lesiones escamosas intraepiteliales de alto grado (CIN 2/3, HSIL) y a cáncer de cuello uterino. Algunos de los tipos virales de alto riesgo están también asociados a tumores en otras localizaciones ano-genitales. Más del 90% de los cánceres de ano son producidos por el VPH. Una fracción considerable de las infecciones por VPH es autolimitada, particularmente las que se asocian a variaciones morfológicas de tipo CIN 1 / 2. Los VPHs de tipo 6/11 rara vez se encuentran en lesiones neoplásicas cervicales y cursan predominantemente con infecciones clínicamente visibles, denominadas condilomas acuminados (CA). Ocasionalmente, las infecciones por VPH se transmiten de la madre al recién nacido abocando a infecciones del tracto respiratorio superior y ocasionando una rara entidad clínica denominada papilomatosis laríngea.
El sexo oral también tiene sus riesgos: Está demostrado que el 26% de las esofagitis están producidas por HPV (DNA positivo), el 88% de los adenocalcinomas de esófago igualmente, así como el 96% de los esófagos de Barret.
· Historia natural de las infecciones por VPH:
Tanto la mujer como el hombre pueden ser portadores asintomáticos y vehículos de la infección genital por VPH. La transmisión se produce por contactos sexuales y los órganos más susceptibles de infección con potencial de iniciar una transformación neoplásica son el cuello uterino (zona de transición), la línea pectinea del canal anal, garganta y boca. Las infecciones por VPH son frecuentemente en sábana (sembrada), en cuyos casos el ADN viral puede recuperarse del cuello uterino, vulva, vagina, canal anal, garganta, boca, pene y escroto. Socialmente pueden identificarse grupos de alta prevalencia en la población que ejerce la prostitución, en la población reclusa asociada al consumo de drogas y en los grupos infectados por el virus de la inmunodeficiencia humana (VIH).
Una de las razones por las que este tipo de infecciones ha cobrado un gran interés reside en la asociación etiológica de algunas de estas infecciones con el carcinoma de cuello uterino y con otros tumores del tracto ano-genital masculino y femenino.
La prevalencia de ADN de VPH está asociada a la edad. Generalmente, la prevalencia es más alta en las edades inmediatas al inicio de las relaciones sexuales y responde al patrón de comportamiento sexual de la comunidad. En las poblaciones donde el número de compañeros sexuales distintos y ocasionales es elevado, la prevalencia puede ser tan elevada como del 30-40% en los grupos de 15 a 25 años de edad. El primer pico de prevalencia va seguido por una disminución muy marcada, de modo que en las edades intermedias 25-40 años la detección viral se estabiliza a niveles de entre el 3 y el 10%. Esta fracción prevalente se interpreta como medida indirecta del grupo de mujeres portadoras crónicas de la infección viral y del grupo de alto riesgo para la progresión neoplásica. En algunas poblaciones, se ha observado un segundo pico de prevalencia en las mujeres post-menopáusicas cuya interpretación es todavía objeto de investigación.
· Tipos de VPH
Se han identificado mas de 200 genotipos de HPV. La mayoría de estas infecciones si no progresan a cáncer, al cabo de dos años desaparecen si no hay reinfección.
- Alto Riesgo
16, 18, 26, 31, 33, 35, 39, 45, 51, 52, 53, 56, 58, 59, 62, 66, 67, 68, 69, 70, 71, 73, 82, 83, 84, 85 y 89.
El HPV 56 y el HPV 51 presentan una frecuencia en los exudado anogenitales del 5,8% y 7,1% (10.1016/jamog.2007.09.001). Se ha encontrado en un 74% de los canceres colorectal ADN del HPV. Más frecuente en el cáncer rectal que en el colon. La vía de contagio del HPV en la mucosa colorectal en pacientes que no han tenido coito anal, se piensa que es una transmisión retrógrada del HPV vaginal a través del perineo hacia el tracto grastointestinal, ya que el virus HPV permanece varios años en la piel. Nunca se debe hacer un exudado vaginal y rectal con la misma torunda. El VPH se ha encontrado en el 90% de los canceres de ano, pene, orofaringeo, amigdalar y en cáncer de la base de la lengua, tanto en hombres como en mujeres. - Bajo Riesgo
6, 11, 32, 40, 42, 43, 44, 54, 55, 57, 61, 64, 72, 74, 81, 87 y 91.
¿Qué hacer si la prueba del HPV da positivo?
- Pensar que entre el 80% y 85% de los casos tu organismo elimina el virus, es decir desaparece por sí solo.
- Si la citología cervicovaginal o Papanicolau da negativo, es decir que no hay ninguna célula maligna, no debes preocuparte. Se aconseja efectuar dentro de los siguientes seis meses nueva citología y estudio del HPV.
- Si la citología presenta alguna lesión precancerosa o cancerosa como las que se indican en el apartado siguiente, dependiendo de la edad y la paridad de la paciente se tomará una u otra decisión, que puede ser de índole quirúrgica o bien seguimiento del desarrollo de la enfermedad. Teniendo en cuenta que cada paciente es único. De cualquier forma a los seis meses se recomienda repetir citología y estudio de HPV.
- En el varón por la anatomía del aparato reproductor, uretra de 17 cm. con nichos y glándulas parauretrales, se puede detectar el HPV efectuando entre 8 y 10 estudios del semen en distintos días, ya que, si el estudio se realiza solamente una vez da un 60 % de falsos negativos. Únicamente mediante el estudio seriado se puede llegar a la detección completa. Si el varón a pesar de ser portador no presenta ninguna lesión se aconseja seguimiento. Si presenta alguna lesión se efectúa estudio anatomopatológico y según los resultados cirugía si procede.
¿Qué hacer si tengo relaciones anales y el HPV ha dado positivo?
- Efectuar PCR HPV en Ano. Si éste es positivo efectuar citología anal. Ambas pruebas deben ser efectuadas por persona cualificada. Si no la encuentras puedes pedir consejo en el correo abajo indicado.
- El cáncer de ano está producido en el 100% de los casos por el Virus del Papiloma Humano.
- En persona inmunodeprimidas (sida, sifilis, hepatitis etc..) los condilomas, que teóricamente no son cancerígenos, en estos pacientes si lo son.
**** Para cualquier consulta puede dirigirse a: aegoas@gmail.com
· Etapas clínicas:
En el cuadro 1 y 2, se encuentra el sistema de clasificación por etapas actual de la Federación Internacional de Ginecología y Obstetricia (FIGO). Cuando hay dudas en relación con la etapa que debe atribuirse al cáncer, es obligatorio seleccionar la etapa previa. Después de asignar una etapa clínica y de haber iniciado el tratamiento, no debe cambiarse de etapa porque los datos subsecuentes pueden extender la clasificación por etapas clínica o quirúrgica. El “aumento de la etapa” del problema de las pacientes durante el tratamiento producirá una mejoría errónea en los resultados del mismo en caso de enfermedad de etapa baja. A continuación se presenta un desglose de la incidencia del cáncer cervicouterino según la etapa en el momento del diagnostico: 38% etapa I, 32% etapa II, 26% etapa III y 4% etapa IV.
Clasificación por etapas de la FIGO del carcinoma del cuello uterino.
Carcinoma preinvasivo
- Etapa I :Carcinoma confinado estrictamente al cuello uterino (no debe tomarse en cuenta la extensión hacia el cuerpo uterino)
- Etapa II: El carcinoma se extiende más allá del cuello uterino, pero no se ha extendido hasta la pared. El carcinoma abarca la vagina, pero no al tercio inferior de ésta.
- Etapa IIa: No hay afección parametrial manifiesta.
- Etapa IIb: Hay afección parametrial manifiesta.
- Etapa III: El carcinoma se ha extendido hasta la pared pélvica. Al examen rectal no se encuentra un espacio libre de cáncer entre el tumor y la pared pélvica. El tumor abarca al tercio inferior de la vagina. Todos los casos tienen hidronefrosis o riñón no funcional.
- Etapa IIIa: No hay extensión hacia la pared pélvica.
- Etapa IIIb: Extensión hacia la pared pélvica, hidronefrosis o riñón no funcional, o una combinación de estos problemas.
- Etapa IV: El carcinoma se ha extendido más allá de la pelvis verdadera o afecta desde el punto de vista clínico a la mucosa de vejiga o recto. El edema buloso, como tal, no permite que un caso se adjudique a la etapa IV.
- Etapa IVa: Extensión del crecimiento hacia los órganos adyacentes.
- Etapa IVb: Extensión hasta los órganos a distancia.
I. El diagnostico de las etapas Ia1 y Ia2 debe basarse en el examen microscópico del tejido resecado, de preferencia un cono, que debe incluir a todo la lesión. La profundidad de la invasión no debe pasar de 5 mm a partir de la base del epitelio, sea superficial o glandular, en el cual se origina. La segunda dimensión, la diseminación horizontal, no debe ser mayor de 7 mm. La afección del espacio vascular, sea venoso o linfático, no debe alterar la clasificación de la etapa, pero se registrará de manera especifica puesto que puede afectar a las decisiones terapéutica futuras. Las lesiones de mayor tamaño deben clasificarse como de etapa Ib. Como regla, es imposible estimar desde el punto de vista clínico si un cáncer del cuello uterino se ha extendido hasta el cuerpo del útero. Por tanto no debe considerarse la extensión hacia el cuerpo uterino.
II. La paciente con un crecimiento fijo a la pared pélvica lateral por medio de un parametrio corto e indurado, pero no nodular, debe adjudicarse a la etapa IIb. Durante el examen clínico, es imposible decidir si un parametrio liso e indurado es, en realidad canceroso o sólo inflamatorio. Por tanto, el caso debe asignarse a la etapa III solo si el parametrio es nodular hasta la pared pélvica o el propio crecimiento se extiende hasta esta pared.
III. La presencia de hidronefrosis o de riñón no funcional a causa de estenosis del uréter por el cáncer permite que el caso se adjudique a la etapa III incluso si, según otras observaciones, debe adjudicarse a las etapas I o II.
IV. La presencia de edema buloso, como tal, no debe permitir que el caso se adjudique a la etapa IV. Los rebordes y los repliegues en la pared vesical no deben interpretarse como signos de afección submucosa de la vejiga si se conservan fijos al crecimiento en el momento de la palpación (es decir, en el examen desde la vagina o el recto durante la cistoscopia). El descubrimiento citológico de células malignas en los lavados provenientes de vejiga requiere investigación más a fondo y obtención de una biopsia de la pared de la vejiga.
FIGO, Federación Internacional de Ginecología y Obstetricia.
Preguntas asociadas al VPH
Si este virus es una enfermedad de transmisión sexual ¿cómo es posible encontrarlo antes de la coitarquia (primer coito o copula) o en niños?. A pesar de que se sabe poco de la vía de transmisión hay evidencias que demuestran transmisión vertical durante el embarazo (transmisión transplacentaria y vía líquido amniótico) y canal del parto (vía mucosa cervical y vaginal). Después del parto por transmisión horizontal via autoinoculacion o heteroinoculacion a través de contacto directo o de fómites (cualquier sustancia que puede absorber y luego transmitir agentes infecciosos, baño, cambio de pañales u otros tipos de contacto directo o indirecto), en este caso el agente infeccioso es el virus del papiloma humano.
Para más información sobre este tema ver artículo «Sex Transim Infect. 2016,92 (1) 19-23».
Los abusos sexuales en niños también. es otro medio de transmisión del VPH.
Hasta un 17% de mujeres con citología cervicovaginal (Papanicolau) normal, presentaban una infección por el VPH. En estudios complementarios el 15% de las infectadas por el virus, progresa a cáncer escamoso. En España cada año 2.100 mujeres desarrollan cáncer de cérvix invasivo, de las cuales, unas 1500 acaban muriendo por esta enfermedad.
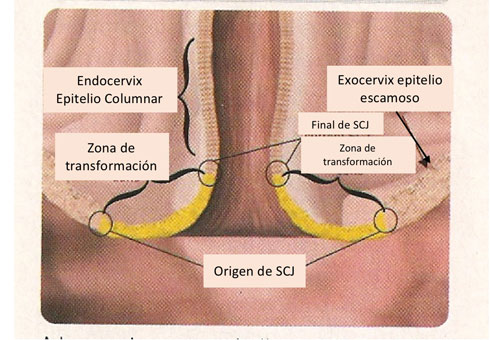
transformación de la unión escamosa columnar ( SCJ)
· Vacunas
En España en el Centro de Farmacovigilancia de Madrid las reacciones adversas sospechosas de ser producidas por la vacuna de VPH son: Alteraciones del nivel de conciencia. Cefaleas, crisis tonicoclónicas generalizadas, crisis y transtornos convulsivos, purpura y enfermedades relacionadas, signos y síntomas neurológicos, síntomas y signos del oído interno, sintomatología asociada a naúseas y vómitos, temblor (excluído el congénito), trastornos asténicos, trastornos febriles, trastornos por debilidad muscular, sincopes(algunos acompañados de cuadros de convulsion, convulsion clónica, epilepsia y convulsion de gran mal. Se han descrito también cuadros de mareo sin que se acompañe de sincope.
El ministerio de Sanidad del Japón no recomienda la vacunación contra el virus del papiloma humano por sus efectos adversos. En Francia la Comisión Regional de Indemnizaciones de Accidentes Médicos de Aquitania ha reconocido la relación de causalidad de la vacuna del papiloma humano con daños en el sistema inmune en una chica de 15 años. Esta paciente aparte de encefalomielitis aguda,ha atravesado fases de ceguera, parálisis facial y se encuentra desde hace meses parapléjica. En Suecia la HTA (Health Technology Assessments) dice que no hay evidencia científica suficiente para recomendar la vacuna contra el VPH.
Los efectos secundarios adversos graves ESAG (generalmente son reacciones autoinmunes debilitantes, que dejan minusvalías) que se han encontrado en los estudios que se han efectuado en adultos sanos, a los que se les ha administrado cualquiera de las dos vacunas actualmente en el mercado son de entre 2.300 a 2.880 ESAG/ por cada 100.000 pacientes. Se puede ver en la Agencia Europea del Medicamento000721/WC500024636.Antes se nos decia que eran seguras. Ahora nos dicen que la ratio riesgo beneficio es positivo.
Para solicitar más información acerca de los efectos secundarios de esta vacuna se pueden dirigir a: ASOCIACION ESPAÑOLA DE AFECTADOS VACUNA VIRUS PAPILOMA HUMANO teléfono 699.267.508.
En España la campaña contra la vacuna del VPH la lidera el Dr Carlos Alvarez Dardet profesor en Alicante. En el Reino Unido se ha formado la AHVID UK Association of HPV Vaccine Injured Daugthers. En Dinamarca su gobierno no se ha creido, por falso, el informe emitido por la EMA (European Medicine Agency) y los laboratorios que fabrican dichas vacunas, y ha puesto un millón de euros para que su ministerio de Sanidad investigue los efectos secundarios sufridos por las 1.300 niñas danesas afectadas por la vacuna del HPV.
Nos hace dudar de la inmunogenicidad de la vacuna, el hecho de haber encontrado alteraciones celulares producidas por el mismo genotipo HPV en mujeres que teóricamente habían sido vacunadas.
En dos años el 57% de los pacientes con CIN/1 vuelven a la normalidad, el 32% persiste la lesión, un 10% progresan a carcinoma in situ y un 1% a cáncer invasivo.
En dos años el 50% de los pacientes con CIN/2 vuelve a la normalidad. En el 32% de los casos persiste y en 18% progresa a CIN/3 o a cáncer. Este puede ser carcinoma de células escamosas que el 75% de los casos y el 25% son adenocarcinomas. De las células glandulares del endocérvix.
En dos años los pacientes con CIN/3 el 32% vuelve a la normalidad, persiste en menos del 56% y en más del 12% progresan a cáncer de cérvix in situ o invasivo.
La progresión depende de la edad de la paciente y de la carga vírica del VPH.